El gluten en los medicamentos
El gluten en los medicamentos.
Es por todos conocido que el gluten se puede encontrar en los alimentos de muchas maneras.
Pero lo que mucha gente desconoce es que también lo podemos encontrar en algunos productos de cosmética y en los medicamentos, ya que el almidón es un excipiente altamente utilizado en la fabricación de cápsulas y pastillas.
Sabemos que por encima dede 20ppm, los celiacos no podemos consumir nada que lo contenga: ni alimentos ni medicamentos.
Legislación gluten y medicamentos
El artículo 34 del Real Decreto 1345/2007 de 11 de octubre, regula todos los medicamentos fabricados industrialmente y deja constancia de la declaración obligatoria de la presencia como excipiente de almidón de trigo, avena, cebada, centeno, o triticale y sus derivados, en el prospecto, la ficha técnica y el etiquetado del mismo.
Además, la Circular 01/2018 de la Agencia Española de Medicamentos y Productos Sanitarios estipula que se debe facilitar la siguiente información:
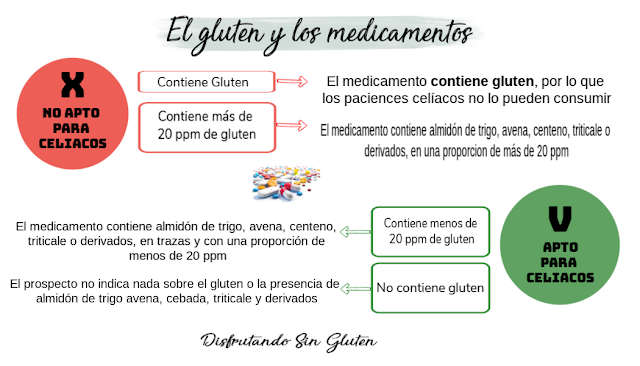
- – Si el medicamento contiene menos de 20 ppm de gluten, se declarará su presencia, pero también se indicará: “es adecuado para pacientes celiacos” y “los pacientes con alergia a X (distinta de la EC) no deben tomar este medicamento”.
- – Si el medicamento contiene más de 20 ppm se incluirá la siguiente información: “este medicamento contiene almidón de X, que equivale a “x” ppm de gluten, lo que debe ser tenido en cuenta por los pacientes celiacos”, “los pacientes con alergia a X (distinta de la EC) no deben tomar este medicamento.”
Con toda esta información, si leemos bien el prospecto de cualquier medicamento, está claro si lo podemos tomar o no y ante cualquier duda, hay que consultar al farmacéutico de confianza.
El gluten como tal no suele aparecer, sino el nombre del excipiente que lo contiene.
Por ello pinchando este enlace aparece el listado de los excipientes que pueden contener gluten y ante los que debemos estar alerta.

Si entráis en la web de la Agencia Española del Medicamento, podéis consultar directamente a través del nombre del medicamento, sus excipientes.
Con respecto a los medicamentos genéricos, hay empresas como CINFA que tienen sus listados propios de medicamentos sin gluten.
Como os decía antes, consultad a vuestro farmacéutico de confianza para aseguraos.
Espero que el post os haya resultado de utilidad y mirad siempre el prospecto antes de consumir ningún medicamento.
Helena
INFO: Post con información extraída de FACE y de Agencia Española del Medicamento.



